Exelixis公司宣布,FDA已接受审查该公司抗癌药cabozantinib的新药申请(NDA),该药用于不能手术切除的恶性局部晚期或转移性髓样甲状腺癌(medullary thyroid cancer,MTC)的治疗。同时,FDA已授予该药优先审查资格(priority review designation),这意味着FDA将在6个月内完成cabozantinib NDA的审查。
在今年5月份,Exelixis向FDA提交了cabozantinib的新药申请,同时还向FDA提起优先审查申请。
临床前研究表明,cabozantinib通过靶向抑制MET、VEGFR2 及RET信号通路而发挥抗肿瘤作用,它能够杀死肿瘤细胞,减少转移并抑制血管生成。
Cabozantinib III期临床试验EXAM在FDA的特殊评估协议(SPA)下进行,以无进展生存期(PFS)为主要终末点。
2011年12月,Exelixis公布了EXAM研究结果,与安慰剂相比,cabozantinib使患者的中位无进展生存期增加了7.2个月,增至11.2月。
(责任编辑:张万青)
39健康网(www.39.net)专稿,未经书面授权请勿转载。

 39健康网
39健康网 突破!国产抗癌药“饿死”癌细胞,或可治多种癌症,有望在美上市
突破!国产抗癌药“饿死”癌细胞,或可治多种癌症,有望在美上市 好消息!17种抗癌药被纳入医保,最高降幅达71%
好消息!17种抗癌药被纳入医保,最高降幅达71% 120万一针的“抗癌药”到底能治哪些肿瘤?血液科主任道出真相
120万一针的“抗癌药”到底能治哪些肿瘤?血液科主任道出真相 今年又有8种抗癌药进入医保,省钱还能救命!有你在用的吗?
今年又有8种抗癌药进入医保,省钱还能救命!有你在用的吗? 治愈率75%的广谱抗癌药真的存在?其实是这样的...
治愈率75%的广谱抗癌药真的存在?其实是这样的...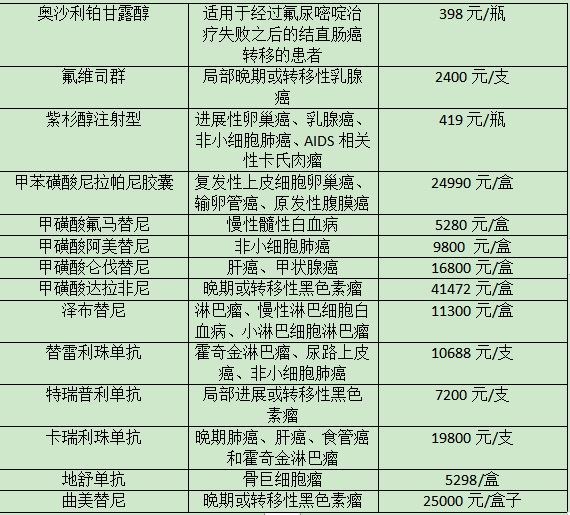 医保目录更新:14种抗癌药降价,4大国产PD-1全部纳入!
医保目录更新:14种抗癌药降价,4大国产PD-1全部纳入! 治疗关节炎该怎么用药?
治疗关节炎该怎么用药? 万万没想到,“神药”二甲双胍会在这“小病”遇滑铁卢?
万万没想到,“神药”二甲双胍会在这“小病”遇滑铁卢? 图说药用辅料的巨大市场
图说药用辅料的巨大市场 再添证据!减肥“神药”索马鲁特每周一次的最佳剂量来了!
再添证据!减肥“神药”索马鲁特每周一次的最佳剂量来了!



















